1. はじめに
顕微鏡で細胞を観察するとき、皆さんはどんな「色」を思い浮かべるでしょうか?緑色に光るタンパク質、赤く染まった核、青く標識された細胞膜——生命科学の世界では、こうした「色分け」が研究の成否を握る重要な鍵となっています。
それぞれのタンパク質がどこにいて、どのように相互作用しているのかを知りたい——そんなとき、研究者たちは異なる色の蛍光色素で目印をつけ、顕微鏡で「色分けして見る」という方法を使います。しかし、従来のレーザー走査型顕微鏡では、「たくさんの色を同時に見分ける」ことと「より細かい構造まで見る(超解像)」ことを、同時に実現するのが非常に困難でした。検出器の構造的な限界や、システムが複雑になりすぎてコストが跳ね上がってしまうことが、大きな壁となっていました。
近年、この難題を解決する革新的な技術が次々と登場し、特許として出願されています。特に注目されているのが、SPAD(単一光子アバランシェダイオード)アレイ検出器とISM(画像走査顕微鏡法)技術を組み合わせた新しいアプローチです。
本記事では、こうした最先端の技術がどのように「色分け」と「超解像」の両立という課題を乗り越えようとしているのか、最新の特許動向とともにわかりやすく解説していきます。
2. レーザー走査型顕微鏡の進化
2-1. 共焦点顕微鏡の基本原理
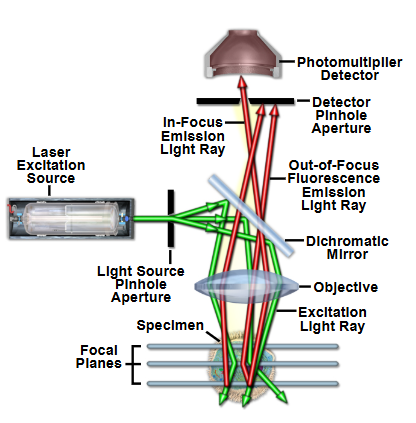
共焦点レーザー走査顕微鏡(CLSM)は、レーザー光を試料上の1点に集光し、その点を走査することで画像を構築します。試料から発せられた蛍光は、ピンホールを通過することで焦点面外からの光を除去し、高コントラストな画像を得ることができます。この「空間フィルタリング」こそが、共焦点顕微鏡の最大の特徴です。
2-2. スペクトルイメージングの必要性
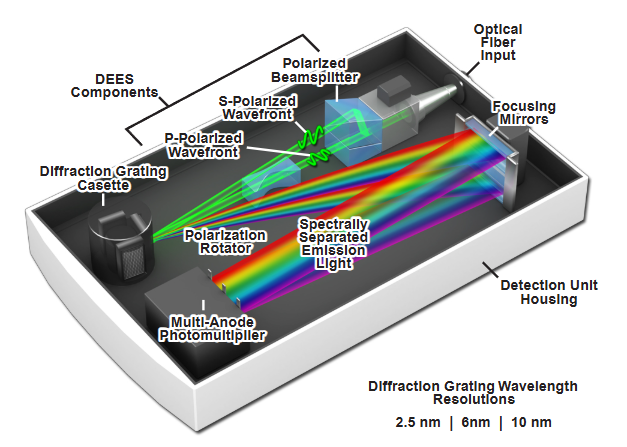
従来の顕微鏡は、特定の波長帯域のみを検出する「波長選択フィルター」を使用していました。しかし、この方法では、スペクトルが重なり合う複数の蛍光色素を同時に検出することが困難でした。スペクトルイメージングでは、発光スペクトル全体を記録することで、後からコンピュータ上で各色素の信号を分離できます。この技術により、多色同時観察の精度が飛躍的に向上しました。
2-3. 従来システムの限界
従来のLSMでスペクトルイメージングと超解像イメージングを同時に実現しようとすると、以下の課題が生じます。第一に、スペクトル検出器(例えば分光器)と超解像用の検出器(例えばカメラ)を両方搭載すると、システムが複雑化しコストが増大します。第二に、光路を分岐させると検出効率が低下し、微弱な蛍光信号を捉えることが困難になります。これらの理由から、市販のLSMシステムでは、スペクトル多チャンネルISM画像を取得することは実質的に不可能でした。
3. 特許から見る技術革新
3-1. SPAD検出器の革新的な読み出し構造(US20170176250A1)
STMicroelectronics社が出願した特許US20170176250A1は、SPAD検出器アレイにおける新しい信号読み出し構造を提案しています。従来のSPADアレイでは、各ピクセルからの信号線が1箇所に集中するため、配線の混雑(routing congestion)が深刻な問題となり、アレイの大型化を妨げていました。
この特許では、「分散型ORツリー構造」を採用することで、各SPADピクセルから出力端子までの信号経路長をすべて等しくし、かつ配線の混雑を大幅に削減しています。具体的には、隣接する2つのSPADピクセルからの信号をOR論理素子で統合し、それらのOR素子を階層的に接続することで、H木構造を形成します。この構造により、アレイサイズを拡大しても信号の遅延や歪みが発生せず、高速かつ高精度な光子検出が可能となります。
SPADアレイは、従来の光電子増倍管(PMT)と比較して小型化が可能であり、ISM技術への応用において大きなアドバンテージを持ちます。この特許技術により、SPAD検出器の実用性が大きく向上し、商用顕微鏡システムへの搭載が現実的なものとなりました。
3-2. 可変焦点距離とスペクトル分離の統合(US9389402B2)
Carl Zeiss Microscopy社の特許US9389402B2は、レーザー走査顕微鏡における「可変倍率」と「スペクトル分離」の同時実現を可能にする光学系を提案しています。この発明の核心は、可変焦点距離の光学系と、制御可能な分散デバイスを組み合わせた検出ユニットにあります。
従来の多焦点LSMでは、複数の焦点からの蛍光を個別に共焦点フィルタリングすることが困難でした。この特許では、2つのスリット状ピンホールを光学的に共役な位置に配置し、その間に画像回転素子を挿入することで、各焦点スポットの画像方位を90度回転させます。これにより、個々の点画像が直交する2方向で独立に共焦点フィルタリングされ、完全な共焦点性が実現します。
さらに、この光学系に分散デバイスを組み込むことで、スペクトル分離とISMを統合したシステムが構築可能となります。この技術により、1台のLSMで、従来は別々のシステムでしか実現できなかったスペクトルイメージングと超解像イメージングを同時に行うことができます。
3-3. 超高速イメージングプラットフォーム(US11714270B2)
テキサス大学システムの特許US11714270B2は、高速レーザー走査顕微鏡における同期制御技術を開示しています。この発明の特徴は、共振ミラーの参照クロック信号を高精度に処理し、ガルバノミラー、データ取得ユニット、z軸ステージの動作を完全に同期させる制御回路にあります。
従来の高速LSMでは、画像のピクセル数やラインの数が固定されているか、限られた選択肢しかありませんでした。これは、ハードウェアの同期制御の限界によるものです。この特許技術では、参照クロック信号を「強化」(ノイズフィルタリング、電圧調整、電流供給)し、さらに周波数を2倍にすることで、極めて柔軟な画像パラメータ設定を可能にしています。
この技術により、研究者は任意のピクセル数(例えば3000×1000ピクセル)や視野サイズを自由に設定でき、従来は不可能だった高アスペクト比試料(例えば線虫C. elegansの全身)の高速3Dイメージングが実現しました。さらに、マイクロ流体デバイスとの組み合わせにより、複数の試料を自動的に撮影する高スループットイメージングも可能となっています。
4. 応用分野と実用化
4-1. 生命科学研究への応用
SPAD検出器とISM技術の統合は、生命科学研究に革命をもたらしています。例えば、カルシウムイメージングでは、神経細胞の活動を蛍光強度の変化として捉えますが、従来の技術では時間分解能と空間分解能を同時に高めることが困難でした。超高速ISMシステムでは、1秒間に数十フレームの超解像画像を取得できるため、神経回路の動的な活動を詳細に観察できます。
また、スペクトルイメージング機能により、複数の蛍光タンパク質を同時に観察し、異なる細胞種や分子間の相互作用をリアルタイムで追跡することが可能になりました。これは、発生生物学や神経科学において特に重要です。
4-2. 創薬研究での活用
創薬研究では、候補化合物が細胞内でどのように作用するかを詳細に観察することが求められます。スペクトル多チャンネルISMにより、薬剤投与後の細胞内での複数のシグナル伝達経路の変化を同時に追跡できます。これにより、薬効メカニズムの解明や副作用の早期発見が可能となり、創薬プロセスの効率化に貢献しています。
4-3. 臨床診断への展開
SPAD検出器の高感度性と高速性は、臨床診断分野でも注目されています。例えば、皮膚の共焦点イメージングでは、メラノーマ(悪性黒色腫)の早期診断に利用されています。SPAD検出器を用いることで、より微弱な蛍光信号を検出でき、従来よりも早期の段階で病変を発見できる可能性があります。
また、手術中のリアルタイム組織診断(光学生検)においても、高速ISM技術は有用です。切除した組織を迅速に観察し、がん細胞の有無を即座に判定することで、手術の精度向上と患者の負担軽減に寄与します。
5. 課題と展望
5-1. 現在の技術的課題
SPAD検出器アレイの最大の課題は、現時点ではピクセル数が限られていることです。市販のSPADアレイは、せいぜい数十×数十ピクセル程度であり、CMOSカメラの数百万ピクセルには遠く及びません。これは、データ転送速度の限界によるものです。各SPADピクセルが光子を検出するたびに信号を出力するため、膨大なデータ量をリアルタイムで処理する必要があります。
また、SPAD検出器は暗電流(光がなくても発生する信号)が比較的大きく、これがノイズ源となります。特に、長時間露光が必要な微弱蛍光の観察では、暗電流の抑制が重要な課題です。冷却機構の搭載により暗電流を低減できますが、システムの複雑化とコスト増加を招きます。
5-2. 研究の最前線
現在、CMOS技術を用いた大面積SPADアレイの開発が進んでいます。最新の研究では、100万ピクセルを超えるSPADアレイが試作されており、近い将来、商用化される見込みです。また、各ピクセルに時間測定回路(TDC: Time-to-Digital Converter)を集積することで、光子の到達時刻をピコ秒の精度で記録できる「フォトンカウンティング検出器」の開発も進んでいます。これにより、蛍光寿命イメージング(FLIM)とISMを同時に実現することが可能になります。
さらに、機械学習を用いた画像処理技術の進展も著しいものがあります。ディープラーニングにより、少ないフォトン数から高品質な超解像画像を再構成する技術が開発されており、SPAD検出器のノイズ問題を補完することが期待されています。
5-3. 未来の展望
今後10年間で、レーザー走査型顕微鏡は大きな変革を遂げるでしょう。SPADアレイ検出器の大型化と低価格化により、スペクトル多チャンネルISMが標準的な機能として搭載されるようになると予想されます。これにより、研究者は複雑な生命現象をより高い時空間分解能で観察でき、新たな発見につながるでしょう。
また、AI支援イメージングの発展により、観察条件の自動最適化や、取得した画像からの自動解析が可能になります。例えば、細胞内の特定のオルガネラを自動的に認識し、その動態を追跡するシステムが実現されるでしょう。
さらに、マイクロ流体デバイスとの統合により、数千個の細胞を自動的に観察し、統計的に有意なデータを短時間で取得できる「ハイスループット顕微鏡」が普及すると考えられます。これは、創薬研究やシステム生物学において特に重要です。
6. 結論
レーザー走査型顕微鏡における検出技術の進歩は、生命科学研究に革命をもたらしています。本記事で紹介したSPADアレイ検出器とISM技術の統合は、従来は両立困難だったスペクトルイメージングと超解像イメージングを同時に実現する道を開きました。
特許US20170176250A1の分散型読み出し構造、US9389402B2の可変焦点距離とスペクトル分離の統合、US11714270B2の超高速同期制御技術は、いずれも次世代顕微鏡システムの中核技術となるでしょう。これらの技術は、生命科学研究だけでなく、創薬や臨床診断の分野においても大きな impact を持ち、人類の健康と福祉の向上に貢献することが期待されます。
「見えない世界を色分けする」技術は、まさに今、新たな段階へと進化しています。
参考文献
テーマに近い関連する特許文献
- US20170176250A1 – “Single photon avalanche diode (SPAD) array including distributed or tree for readout”
https://patents.google.com/patent/US20170176250A1 - US9389402B2 – “Laser scanning microscope”
https://patents.google.com/patent/US9389402B2 - US11714270B2 – “High-speed laser scanning microscopy platform for high-throughput automated 3D imaging and functional volumetric imaging”
https://patents.google.com/patent/US11714270B2
記事を作成するにあたり参考にした文献
- Jo, Y. et al. “Image scanning microscopy based on multifocal metalens spectroscopy.” Light: Science & Applications (2025).
https://www.nature.com/articles/s41377-025-01900-3 - Buttafava, M. et al. “SPAD-based asynchronous-readout array detectors for image-scanning microscopy.” Optica 7, 755-765 (2020).
https://opg.optica.org/abstract.cfm?uri=optica-7-7-755 - Nikon MicroscopyU. “Introductory Confocal Concepts.”
https://www.microscopyu.com/techniques/confocal/introductory-confocal-concepts - Tortarolo, G. et al. “Compact and effective photon-resolved image scanning microscope.” Advanced Photonics 6, 016003 (2024).
https://www.spiedigitallibrary.org/journals/advanced-photonics/volume-6/issue-1/016003/Compact-and-effective-photon-resolved-image-scanning-microscope/10.1117/1.AP.6.1.016003.full
※ 記事は公開されている特許情報および学術研究をもとに作成しています。図版の出典は各図のキャプションに記載しています。


コメント